发布日期:2025-03-17 来源: 浏览量:
癌症治疗是全球医学亟待突破的重大挑战,小分子前药纳米组装体凭借其制备工艺简便、载药量高、可控的药物释放和无载体毒性等优势在癌症治疗领域展现出了广阔的发展前景。但是前药纳米组装体的合理设计仍是一项巨大的挑战。为此,沈阳药科大学无涯创新学院药剂学团队提出了前药纳米组装体的模块化设计概念,极大地加速了药物的优化进程与筛选效率。将药物模块与合适的修饰模块相连构建自组装型前药;在药物模块与修饰模块中间插入响应模块保证母药的智能释放;在前药纳米组装体的表面修饰表面功能化模块以改善其体内命运和肿瘤靶向性。
在模块化设计中,修饰模块在驱动前药稳定组装方面发挥着重要作用。修饰模块的结构和性质会显著影响前药的分子间作用力,以及前药与表面功能化模块的亲和力,进而调节前药纳米组装体的组装、激活和体内命运。鉴于此,本团队深入探究了修饰模块的多个核心属性,包括亲疏水性、碳链长度以及刚柔性等,以期进一步优化前药纳米组装体的性能,为抗癌领域带来更为高效、精准的治疗策略。分别开展如下工作:

研究团队首先探究了修饰模块的长度对前药纳米组装体的影响,以紫杉醇(PTX)为药物模块,以二硫键为响应模块,不同碳链长度(AC12,AC16,AC20,和AC24)的脂肪醇作为修饰模块,构建了4种紫杉醇前药。研究发现,随着碳链长度(AC12,AC16,AC20)的增加,紫杉醇前药间的疏水作用力不断增强,导致其自组装能力逐渐增强。但是,当链长进一步增加到AC24时,前药的疏水作用力过强会导致前药聚集沉淀。同时,碳链长度还会进一步影响前药纳米组装体的释药速率、抗肿瘤活性和耐受性。碳链长度最短的PTX-AC12前药纳米组装体具有最强的氧化还原敏感性,释放PTX的速度最快,细胞毒性最强。但是,血液中的氧化物质导致其在体循环中提前释放出PTX,药动学性质不佳。碳链长度最长的PTX-AC24前药纳米组装体显著改善PTX的药动学行为,但过强的疏水性限制其在肿瘤部位智能激活,导致其抗肿瘤活性不佳。PTX-AC16和PTX-AC20前药纳米组装体则表现出适中的氧化还原敏感性、有效的抗肿瘤活性和良好的耐受性。特别是PTX-AC20前药纳米组装体还表现出优越的自组装能力和较长的体内滞留时间,这为解决化疗药物的疗效和耐受性的矛盾带来了新思路。总的来说,本研究探索了修饰模块中脂肪醇的碳链长度对前药纳米组装体体内外命运的影响,并强调了优化修饰模块的长度在前药纳米组装体合理设计中的重要性。
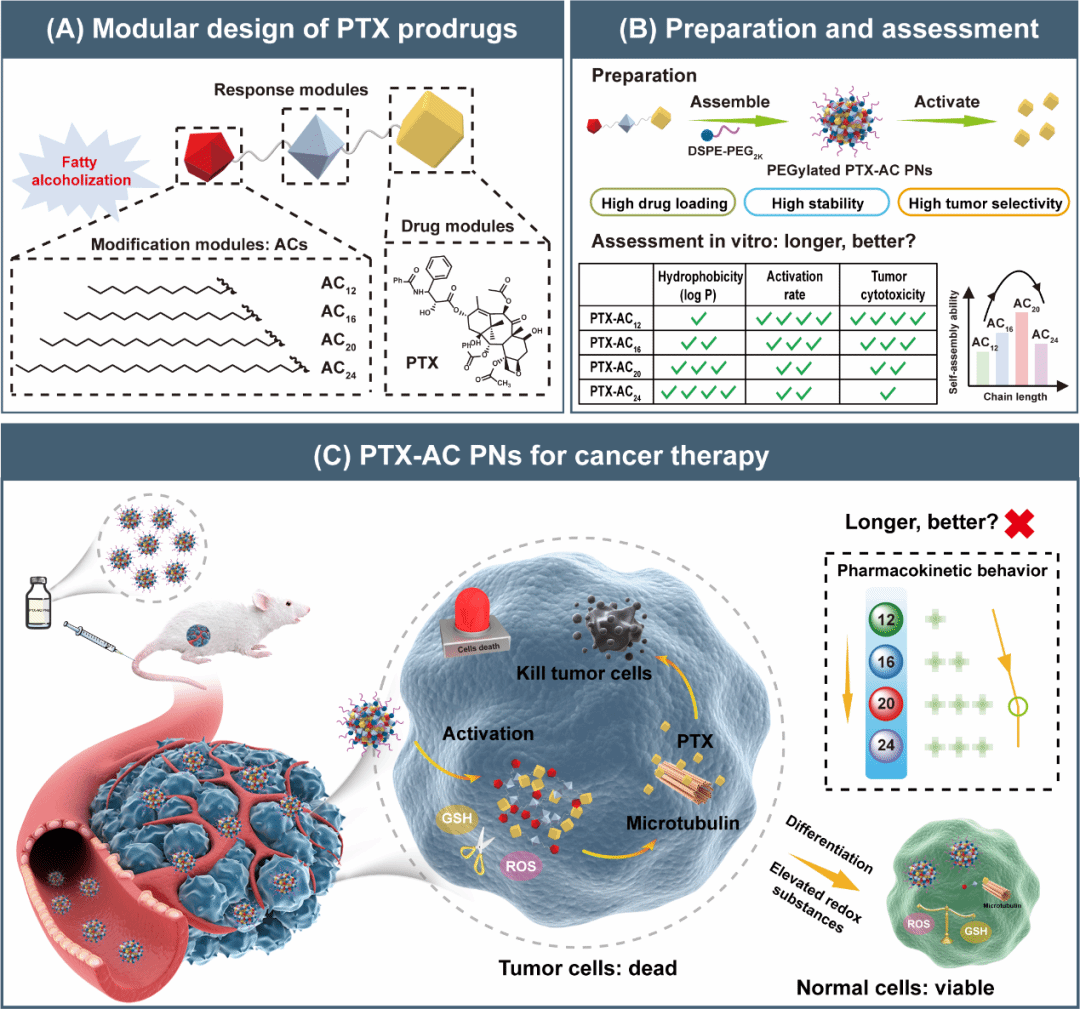
相关研究工作发表在《Journal of Controlled Release》(IF=10.5),题为“Exploring the optimal chain length of modification module in disulfide bond bridged paclitaxel prodrug nanoassemblies for breast tumor treatment”。无涯创新学院2023级博士研究生王丹平和硕士毕业生黄乐童为本文第一作者,孙进教授、孙丙军教授和师资博士后刘钿为本文通讯作者。

通过前面的研究工作,我们发现修饰模块的碳链过短,可能会导致前药的组装稳定性不佳,从而影响其药动学行为;修饰模块的碳链过长则会降低前药的激活效率,导致药效不佳。因此,单纯优化修饰模块的长度难以有效解决这一矛盾问题。研究团队通过进一步文献调研发现,亲水性乙二醇片段可以作为氢键的供体或受体,与水分子形成氢键。那么将乙二醇结构引入修饰模块能否在提高前药组装能力的同时进一步促进相邻化学键的水解,从而实现前药的高效激活?这一问题有待进一步探究。
在这项研究中,研究团队以紫杉醇(PTX)为药物模块,以二硫键为响应模块,乙二醇-油酸作为修饰模块,合成了PTX-SS-OA前药,并以不含乙二醇片段的PTX-SS-OAL前药为对照,深入探究了亲水性乙二醇片段对前药组装性能、药物释放行为和抗肿瘤效果的重要影响。结果表明,亲水性乙二醇片段的引入影响了前药的分子间作用力,增加了前药分子间的氢键作用。此外,亲水性乙二醇片段显著改善了氧化还原药物释放行为,从而进一步影响前药纳米组装体的治疗指数。含有亲水性乙二醇片段的PTX-SS-OA NPs表现出更强的氧化还原敏感性、细胞毒性和抗肿瘤效果。相比之下,尽管不含亲水性乙二醇片段的PTX-SS-OAL NPs的耐受性更好,但其氧化还原敏感性和细胞毒性较弱。这一研究表明亲水性乙二醇片段是调节前药纳米组装体治疗指数的关键因素,探索乙二醇等亲水性片段在药物递送系统中的合理应用,对于开发高效的前药纳米给药系统具有重要意义。
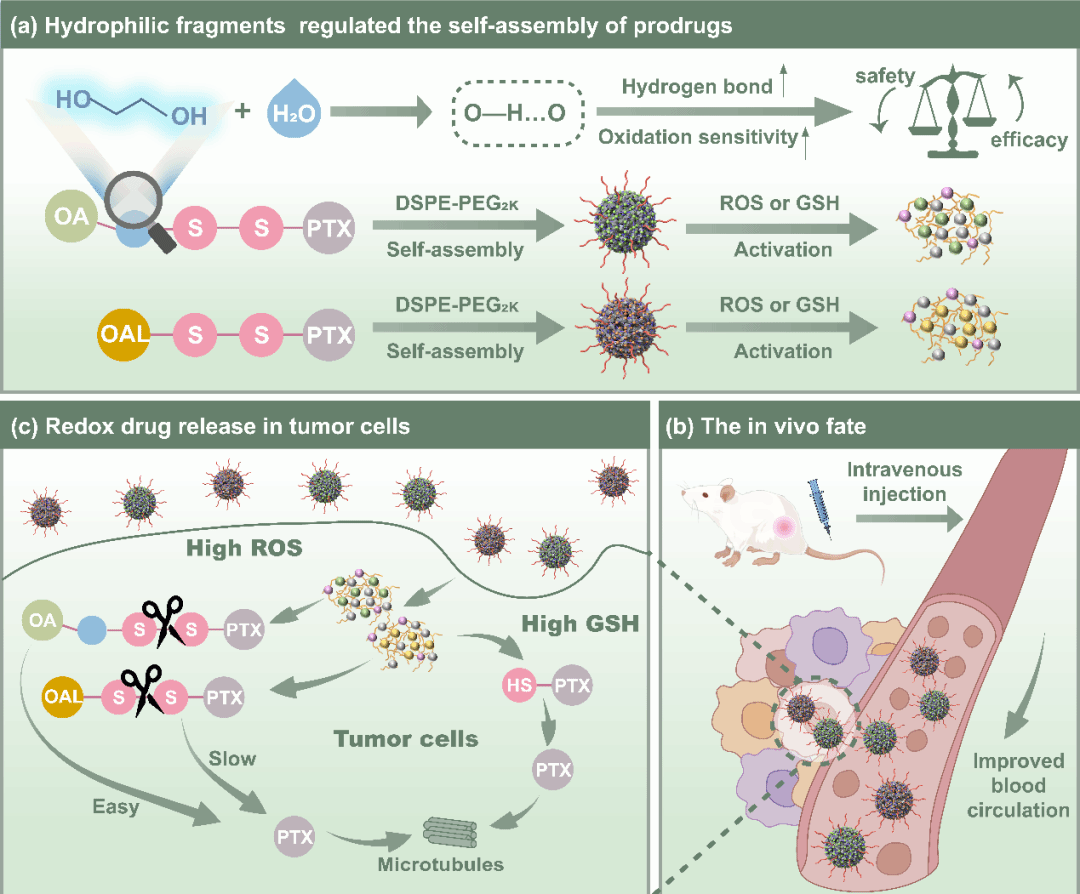
相关研究工作发表在《ACS Central Science》(IF=13.1),题为“Hydrophilic Ethylene Glycol Fragments: A Determinant Affecting the Therapeutic Index of Paclitaxel Prodrug Nanoassemblies”。无涯创新学院2024级博士研究生李雅琪和师资博士后孙一鑫为本文第一作者,孙丙军教授和何仲贵教授为本文通讯作者。

研究团队进一步探究了修饰模块的结构柔韧性对前药纳米组装体的影响。在结构上,修饰模块可被区分为块状和链状两大类,分别以甾醇和脂肪醇为例,两者展现出截然不同的特征:块状模块以其显著的高位阻刚性结构为标志,而链状模块则以其低位阻的柔性链著称。我们推测,柔性支链脂肪醇侧链能更有效地打破前药分子的紧密排列,从而增强其自组装能力。因此,本研究以氧化敏感的硫醚键为响应模块设计了两种灵活度不同的吉西他滨前药纳米组装体(CLS-S-GEM NPs和OD-S-GEM NPs),分别选用刚性结构胆固醇(CLS)和柔性结构2-辛烷基-1-十二醇(OD)作为修饰模块,系统性地考察了修饰模块的灵活度差异对前药纳米组装体构效关系的影响,解析了不同前药纳米组装体在自组装能力、氧化响应释药、体内命运和抗肿瘤疗效等方面的差异。
结果显示,OD-S-GEM具有较强的自组装能力,其纳米组装体展现出了更强的胶体稳定性、母药激活效率和细胞摄取效率,进而对药代动力学和抗肿瘤效果产生了积极影响。体内实验表明,OD-S-GEM NPs在肿瘤部位的有效蓄积和智能释放是其发挥抗肿瘤功效的关键。一方面,OD-S-GEM NPs能够显著改善Cmax和AUC,从而保持了纳米组装体在血流中的结构完整性,并因其更好的稳定性和肿瘤细胞摄取能力而展示出更高的肿瘤蓄积;另一方面,OD-S-GEM NPs因其高氧化敏感性和快速释放特性,在两种小鼠肿瘤模型中展现出与吉西他滨溶液剂相当甚至更优的抗肿瘤疗效。总体而言,本研究强调了修饰模块结构柔韧性对前药纳米组装体的影响。

相关研究工作发表在《Journal of Colloid And Interface Science》(IF=9.4),题为“Revealing the Impact of Modified Modules Flexibility on Gemcitabine Prodrug Nanoassemblies for Effective Cancer Therapy”。无涯创新学院2023级硕士研究生郭嘉煜、硕士毕业生张笑笑和博士毕业生董付丹为本文第一作者,孙丙军教授和姜琪坤特聘教授为本文通讯作者。

与前面构建的以紫杉醇和吉西他滨为药物模块的前药纳米组装体有所不同,蒽环类抗肿瘤药物的结构中通常含有带正电荷的氨基,使得其自组装形成表面带正电荷的纳米组装体,导致其在血液循环中易被吞噬清除。因此,利用带有负电荷的表面功能化模块对带有正电荷的前药纳米组装体进行修饰,有望延长其血液循环时间。在众多带负电荷的载体材料中,胆固醇衍生物是经胆固醇分子修饰或代谢产生的化合物,具有良好的生物相容性。其结构上通常含有疏水的甾体结构以及带负电荷的硫酸基团或羧酸基团,具有较强的疏水性。然而,具有一定亲水性的蒽环类药物与疏水性的胆固醇衍生物仅通过静电作用力难以形成稳定的纳米组装体。因此,增强带正电荷药物的疏水性有望进一步提高两者之间的亲和性,进而提高前药纳米组装体的稳定性。
基于此,研究团队利用酸敏感酰腙键(响应模块)将阿霉素(DOX)与疏水性的肉豆蔻酸(修饰模块)相连构建阿霉素前药(DOX-C14),以提高阿霉素的疏水性。进一步将DOX-C14与6种带有负电荷的胆固醇衍生物以不同摩尔比共组装,以筛选最优的阿霉素前药纳米组装体。结果表明,在静电作用和疏水作用下,DOX-C14与胆固醇硫酸钠以摩尔比1:2(DOX-C14-SCS (1:2))和1:3(DOX-C14-SCS (1:3))的比例所形成的纳米组装体的制剂学性质最好。随后,我们分别利用DSPE-PEG2k或CHOL-PEG2k对DOX-C14-SCS (1:2)和DOX-C14-SCS (1:3)进行表面修饰,进一步提高前药纳米组装体的稳定性和药动学行为。所制得的前药纳米组装体能够有效的蓄积在肿瘤部位,并在肿瘤酸性微环境的刺激下释放DOX发挥抗肿瘤作用。即使在非常高的剂量下(相当于10 mg/kg DOX),对正常组织也没有明显的毒性,显示出较好的肿瘤选择性。
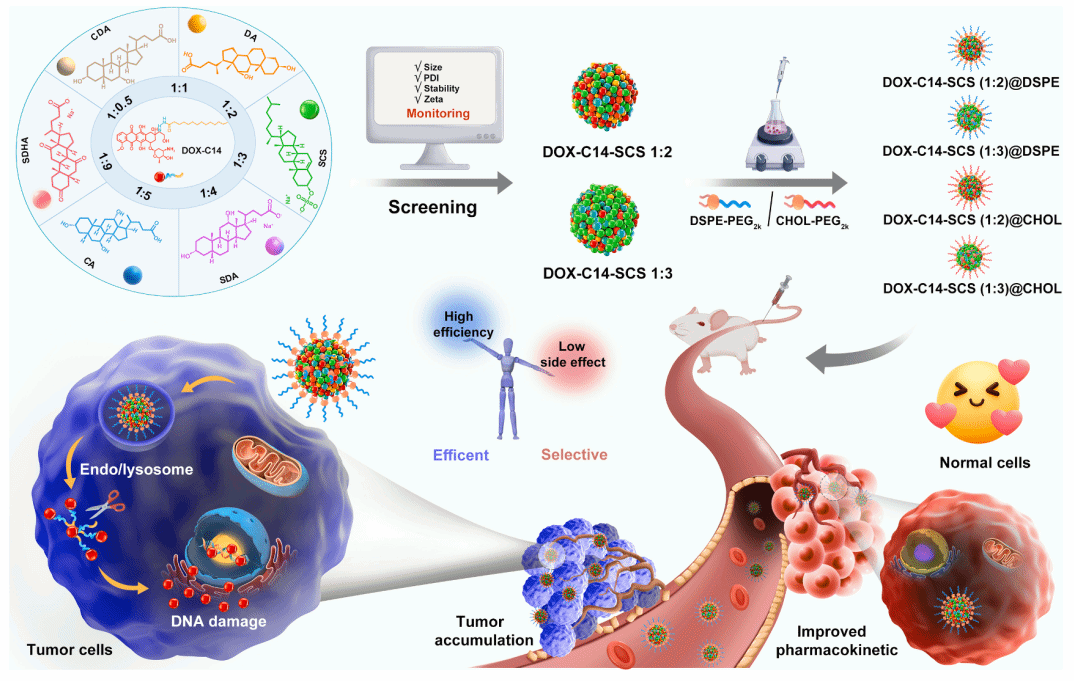
相关研究工作发表在《Chemical Engineering Journal》(IF=13.4),题为“Optimizing the stable doxorubicin prodrug nanocomplex for efficient and selective cancer therapy”。无涯创新学院2022级硕士研究生肖红英为本文第一作者,孙丙军教授、丁怀伟教授和师资博士后李凌霄为本文通讯作者。

在上一项研究工作中,我们发现胆固醇硫酸钠作为表面功能化模块可以显著改善阿霉素前药纳米组装体的稳定性和体内外命运。在本项工作中,研究团队进一步利用疏水性的脂肪醇作为修饰模块与米托蒽醌偶联,提高其与疏水性胆固醇硫酸钠的亲和性,并深入探索修饰模块的链长对米托蒽醌前药与胆固醇硫酸钠亲和力的影响以构建稳定的前药纳米组装体。研究团队通过二硫键将米托蒽醌(MTO)分别与八醇(C8)、十二醇(C12)和十六醇(C16)连接,合成了不同碳链长度脂肪醇修饰的米托蒽醌前药。通过探头超声法制备米托蒽醌前药-胆固醇硫酸钠纳米组装体,并进行了处方筛选和优化。结果表明,与米托蒽醌相比,米托蒽醌前药显著提高了与胆固醇硫酸钠的亲和力。此外,在设计的三种米托蒽醌脂肪醇前药中,脂肪醇的碳链长度越长,其与胆固醇硫酸钠的亲和力越强,与胆固醇硫酸钠组装形成的纳米组装体越稳定,进而改善了米托蒽醌的递送效率。在到达肿瘤部位后,米托蒽醌前药纳米组装体能够被肿瘤细胞内高氧化还原态激活,从而发挥高效低毒的治疗作用。
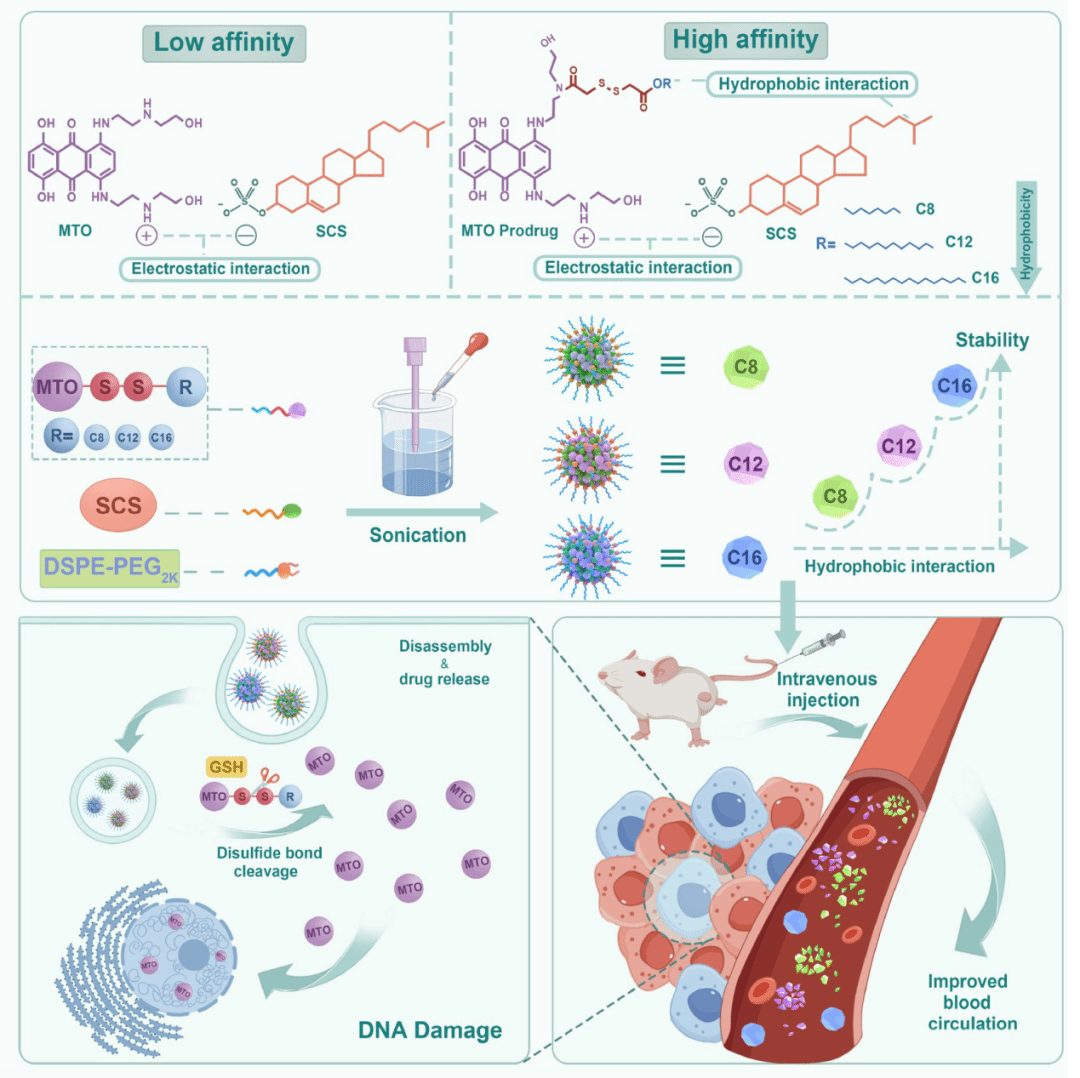
相关研究工作发表在《Science China Chemistry》(IF=10.4),题为“Sodium cholesterol sulfate mediated mitoxantrone prodrug electrostatic nanocomplexes: achieving the therapeutic efficacy and safety of mitoxantrone”。无涯创新学院2021级硕士毕业生赵二伟和师资博士后李凌霄为本文第一作者,孙丙军教授和何仲贵教授为本文通讯作者。



 当前位置:
当前位置: