发布日期:2024-06-09 来源:学科建设办公室 浏览量:
近日,美国化学会旗下期刊《ACS Nano》(IF = 17.1)在线发表了我校药剂学科唐星团队的最新研究成果“Dual-Targeted Self-Adjuvant Heterocyclic Lipidoid@Polyester Hybrid Nanovaccines for Boosting Cancer Immunotherapy”的研究文章。唐星教授、苟靖欣副教授和杨丽教授为本文通讯作者,药剂学2022级博士生刘子旭为本文第一作者,沈阳药科大学为第一通讯单位。
癌症免疫疗法作为一种恢复免疫反应以控制和消除肿瘤的手段,已引起越来越多的关注。树突状细胞(DCs)对T细胞参与的癌症免疫起着至关重要的作用。肿瘤疫苗通过激活DCs引起免疫反应,具有预防和治疗的潜力。然而,肿瘤疫苗也遇到了挑战,尤其是其响应率相对较低。这主要是由于向DCs低效递送、低交叉呈递、DCs内在免疫抑制信号和免疫抑制性肿瘤微环境(TME)等因素造成的。信号转导和转录激活因子3(STAT3)参与多种生物功能,其过度激活与肿瘤进展加速和肿瘤免疫抑制细胞(如Tregs和MDSCs)的上调有关,有助于肿瘤免疫逃逸。此外,STAT3还能抑制DCs的成熟。抗原和STAT3 siRNA的共同免疫可有效促进DCs成熟。该团队之前的研究提供了一种结合STAT3 siRNA和模型抗原(OVA)来增强癌症免疫疗法的策略,STAT3 siRNA与OVA协同作用,促进DCs成熟,提高抗原呈递能力,并减轻免疫抑制(Chemical Engineering Journal 2023, 475, 146474)。因此,在本工作中引入了一种将STAT3 siRNA与疫苗相结合的策略。
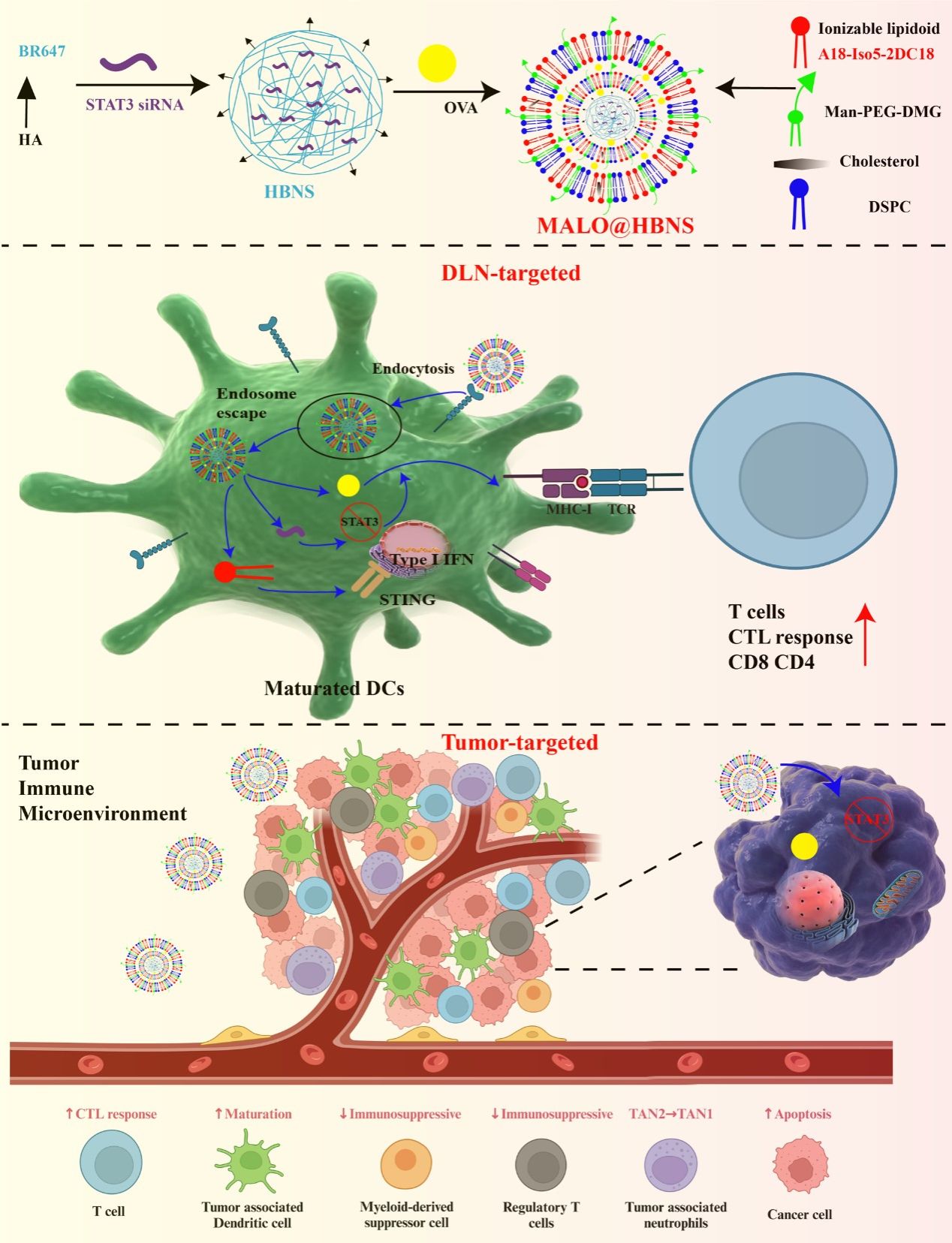
在这项工作中,该团队提出了引流淋巴结(DLN)靶向和肿瘤靶向的纳米疫苗策略。该团队合成了杂环脂质(A18)和聚酯(BR647),以实现癌症的DLN和肿瘤双重靶向免疫治疗。此外,还将寡聚HA和DMG-PEG2000-甘露糖掺入以制备包封OVA和STAT3 siRNA的双靶向纳米疫苗。纳米疫苗旨在以DLN和肿瘤为靶点,有助于将OVA和siRNA运送到细胞质中。这些双靶向纳米疫苗改善了抗原呈递和DCs成熟,激活了干扰素基因刺激器(STING)通路,增强了促凋亡效应,诱导了强大的抗肿瘤免疫反应。此外,这些双靶向纳米疫苗克服了免疫抑制TME,减少了免疫抑制细胞,促进了肿瘤相关中性粒细胞从N2到N1的极化。纳米疫苗改善了抗原交叉呈递,促进了DCs成熟,削弱了TME的免疫抑制作用,增强了促凋亡效应,并激活了STING通路,从而共同推进了癌症免疫疗法。在四种可诱导强大抗肿瘤免疫反应的双靶向纳米疫苗中,杂环类脂@聚酯杂化纳米疫苗(MALO@HBNS)展现了最优异的结果。此外,MALO@HBNS与抗PD-L1抗体的组合策略也显示出了强大的抗癌作用。这项研究提出了一种用于抗肿瘤治疗的双靶向纳米疫苗平台,表明它有可能与免疫检查点阻断剂相结合,成为一种全面的抗癌策略。
该工作得到了国家重点研发计划(NO. 2020YFE0201700)等项目的支持。



 当前位置:
当前位置: